Rituximab and mycophenolate mofetil combination in patients with interstitial lung disease (EVER-ILD): a double-blind, randomised, placebo-controlled trial
Résumé et analyse par Jérémy ANTONIADIS et supervisé par le Pr Brigitte GRANEL
Contexte :
Le traitement de première ligne des pneumopathies interstitielles diffuses (PID) avec un pattern de type pneumopathie interstitielle non spécifique (NSIP) est le Mycophénolate Mofétil (MMF). En cas d’inefficacité ou de rechute le Rituximab est utilisé.
L’essai EVER ILD est un essai de phase 3, randomisé en double aveugle, en groupe parallèle, multicentrique (conduit dans 17 centres académiques Français) évaluant l’efficacité et la sécurité du Rituximab(1000mg, 2 injections à J1 et J15) associé au MMF (2grammes pendant 6 mois) en comparaison au MMF seul, chez les patients atteints de PID associée à une connectivite ou une PID idiopathique (avec ou sans autoimmunité associée) ET un pattern scannographique de type NSIP ou d’une NSIP histologiquement confirmée.
Objectif :
Les auteurs ont voulu évaluer l’efficacité et la sécurité du Rituximab en association au MMF versus le MMF seul chez les patients atteints de PID et présentant un pattern scannographique de type NSIP défini par la présence de réticulation anormales prédominantes au base avec une extension peri-bronchovasculaire et une épargne sous pleural associée à des plages de verre dépoli.
Matériel et méthode :
L’étude portait sur 122 patients âgés de plus de 18 ans atteints de PID associée à une connectivite (23
patients soit 53% avaient une Sclérodermie) ou de PID idiopathique (avec ou sans autoimmunité associée) ET d’un pattern scannographique de type NSIP ou histologiquement confirmée.
Les patients ne devaient pas présenter une autre maladie pulmonaire, ou une autre maladie jugée instable par l’investigateur. Les patients présentant une hypertension artérielle pulmonaire prouvée par un cathétérisme droit et ceux présentant un pattern typique ou probable de pneumopathie interstitielle usuelle ou une histologie avec un pattern différent de NSIP étaient exclus.
Les patients éligibles étaient réfractaires à une première ligne de corticothérapie ou d’un traitement immunosuppresseur ou avaient présenté une rechute de la maladie après traitement.
Le critère de jugement principal était l’évolution du % de la Capacité vitale forcée(CVF) à 6 mois en comparaison à l’état basal. Les critères de jugement secondaires étaient nombreux et incluaient la survie sans progression mesurée après 6 mois. `
Résultats :
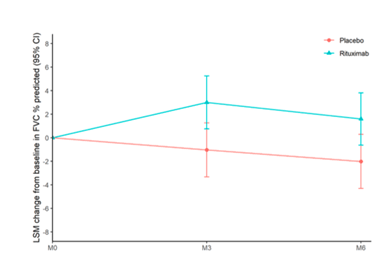
122 patients ont été analysés : 63 dans le groupe Rituximab+MMF et 59 dans le groupe placébo+MMF. Les patients étaient majoritairement des femmes d’âge moyen de 66 ans. A l’état de base, la moyenne de la CVF en % était à 66,7 dans le groupe Rituximab+MMF et 70,2 dans le groupe placébo+MMF. A 6 mois, la CVF% montrait une progression de +1,60 dans le groupe Rituximab+MMF en comparaison à -2,01 dans le groupe placébo+MMF, soit une différence entre groupes de 3,60% [95% CI 0,41 to 6,80]; p=0,0273 (Figure). En volume, la CVF montrait une amélioration dans le groupe Rituximab+MMF de +41mL et une diminution dans le groupe placébo+MMF de -59mL, soit une différence significative entre les deux groupes de 100mL [95% CI 15 à 185], p=0,0207).
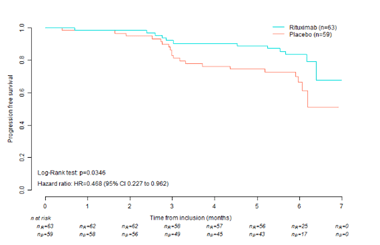
La survie sans progression était meilleure dans le groupe Rituximab+MMF que dans le groupe placébo+MMF, hazard ratio [HR] 0,47 [95% CI 0,23 à 0,96]; p=0,03 (Figure).
Une réduction de l’exposition aux corticoïdes à 6 mois était enregistrée dans le groupe Rituximab+MMF avec 1862mg contre 2314mg dans le groupe placébo+MMF.
Les effets indésirables graves en lien avec le traitement étaient plus fréquents dans le groupe Rituximab+MMF.
Conclusion : Cet article montre que la combinaison Rituximab et MMF augmente la CVF à 6 mois en comparaison au MMF seul avec une différence de 3,6% et de 100 mL sur la CVF à 6 mois chez les patients traités par la combinaison versus MMF seul. Le Rituximab en association au MMF semble être une stratégie raisonnable pour les patients présentant une NSIP. Des études à plus long terme sont nécessaires.







 Association des Sclérodermiques de France
Association des Sclérodermiques de France